北京市医疗器械检验研究院获批18项医疗器械行业标准制修订任务
发布日期:2022-05-27 16:43:16
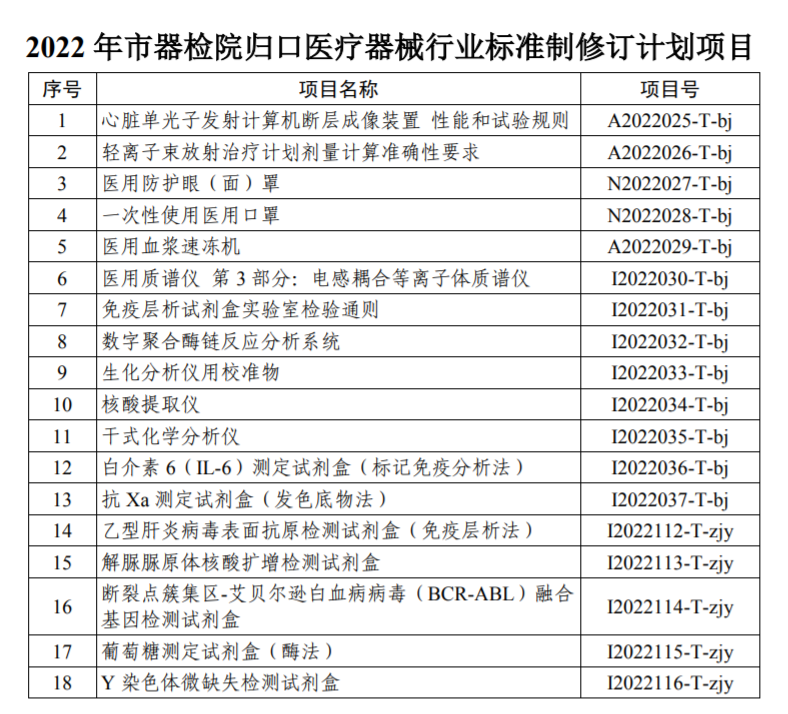
为贯彻国务院办公厅《关于全面加强药品监管能力建设的实施意见》,落实《国家标准化发展纲要》和《“十四五”国家药品安全及促进高质量发展规划》有关要求,近日国家局印发2022年医疗器械行业标准制修订计划项目的通知(药监综械注〔2022〕47号),共下达制修订任务104项,其中市器检院获批18项,占全国任务量17.3%,涉及体外诊断、放射治疗和核医学、实验室医用设备、医用生物防护等医疗器械专业领域。
市器检院归口标委会全年公开征集医疗器械标准计划项目,截至2021年6月,征集到来自医疗器械生产经营企业、使用单位、监管部门、检测机构等单位立项提案100余项,秘书处严格按照立项原则进行立项评估、筛选,将列入国家产业政策、规划、重大科技专项等支持监管和产业发展的提案列入优先项目中。经过前期充分征求意见,调查企业事业组织、社会团体、科研机构等方面的实际需求,对每个项目的必要性和可行性进行评估,对部分条款数据验证等前期准备工作,最终确定上报31项医疗器械行业标准项目,经全社会立项公示征集反馈意见和专家论证会评审,最终获批18项。
随着医疗器械行业新格局加快构建,高质量发展深入实施,产业结构持续优化,市器检院将继续以习近平新时代中国特色社会主义思想为指导,认真落实 “四个最严”要求,按照高质量发展要求做好标准的组织起草、验证、征求意见和技术审查等工作,通过广泛调研、深入研究,借鉴国际标准,确保标准技术内容的科学性、合理性、适用性,坚决守住医疗器械安全底线,进一步提升监管工作科学化、法治化、国际化水平,更好满足人民群众用械安全的需求。